Das AMNOG-Verfahren der frühen Nutzenbewertung und Preisverhandlung neuer Arzneimittel hat sich als weitestgehend funktionsfähiges, lernendes System etabliert. Mit dem GKV-Finanzstabilisierungsgesetz (GKV-FinStG) wurden weitreichende Änderungen beschlossen. Der diesjährige AMNOG-Report beleuchtet die Folgewirkungen.
Seit seiner Einführung im Jahr 2011 wurde das AMNOG-Verfahren mehrfach überarbeitet und auch die aktuelle Regierungskoalition aus SPD, Grünen und FDP kündigte im Dezember 2021 in ihrem Koalitionsvertrag eine „Weiterentwicklung“ an. Ziel war es insbesondere, die Möglichkeiten der Krankenkassen bei der Begrenzung der Arzneimittelpreise zu stärken. Angesichts des Milliardendefizits in der gesetzlichen Krankenversicherung (GKV) wurden diese Absichten im Herbst 2022 mit dem GKV-FinStG konkretisiert und weitreichende strukturelle Änderungen am AMNOG-Verfahren verabschiedet. Der diesjährige AMNOG-Report beschäftigt sich unter Nutzung anonymisierter Abrechnungsdaten der DAK-Gesundheit mit den finanziellen Folgewirkungen des Gesetzes und den absehbaren Umsetzungshindernissen.
Neben der Umsetzung der im Koalitionsvertrag angekündigten Maßnahmen wurde das sogenannte „Orphan-Privileg“ durch Absenkung der bislang geltenden Umsatzschwelle von 50 Millionen Euro auf 30 Millionen Euro eingeschränkt. Fortan werden Arzneimittel zur Behandlung seltener Leiden somit schneller zur Einreichung eines Nutzenbewertungsdossiers verpflichtet. Deutschland ist nach wie vor das einzige Land, das Orphan Drugs im HTA-Prozess entsprechend privilegiert. Die Berechnungen des AMNOG-Reportes beziffern das jährliche Einsparpotenzial der abgesenkten Umsatzschwelle je nach Szenario auf 10 bis 40 Millionen Euro. Das vom Gesetzgeber ausgewiesene Ziel von 100 Millionen Euro pro Jahr dürfte damit zumindest vorerst verfehlt werden.
Dem mit dem GKV-FinStG eingeführten pauschalen Abschlag in Höhe von 20 Prozent auf alle in Kombination abgegebenen Arzneimittel mit neuen Wirkstoffen ging ebenfalls eine längere Diskussion voraus. Allerdings wird ein genereller Abschlag der Herausforderung einer zunehmenden Zahl zugelassener Kombinationstherapien kaum gerecht, denn der medizinische Mehrwert der Kombinationen ist sehr unterschiedlich, was sich auch im Preis widerspiegeln sollte. Bei einem wenigstens beträchtlichen Zusatznutzen wird zwar vom Abschlag ganz abgesehen, aber das ist wenig differenziert. Problematisch erscheint zudem die praktische Umsetzung des Abschlags. Im AMNOG-Report werden deshalb praktische und empirisch fundierte Vorschläge formuliert, wie man diese Umsetzungsschwierigkeiten angehen könnte. Der Report geht zudem der Frage nach, welche Konsequenzen der Abschlag auf Kombinationstherapien haben wird. Die Einsparungen hängen stark von der Art der Umsetzung des Kombinationsabschlags ab – also der Frage, welche Kombinationstherapien am Ende mit einem solchen Abschlag belegt werden. Die Berechnungen ergeben allein in ausgewählten umsatzstarken onkologischen Indikationen (insbesondere Melanom und multiples Myelom) für das Jahr 2021 potenzielle GKV-weite Einsparungen von bis zu 55 Millionen Euro.
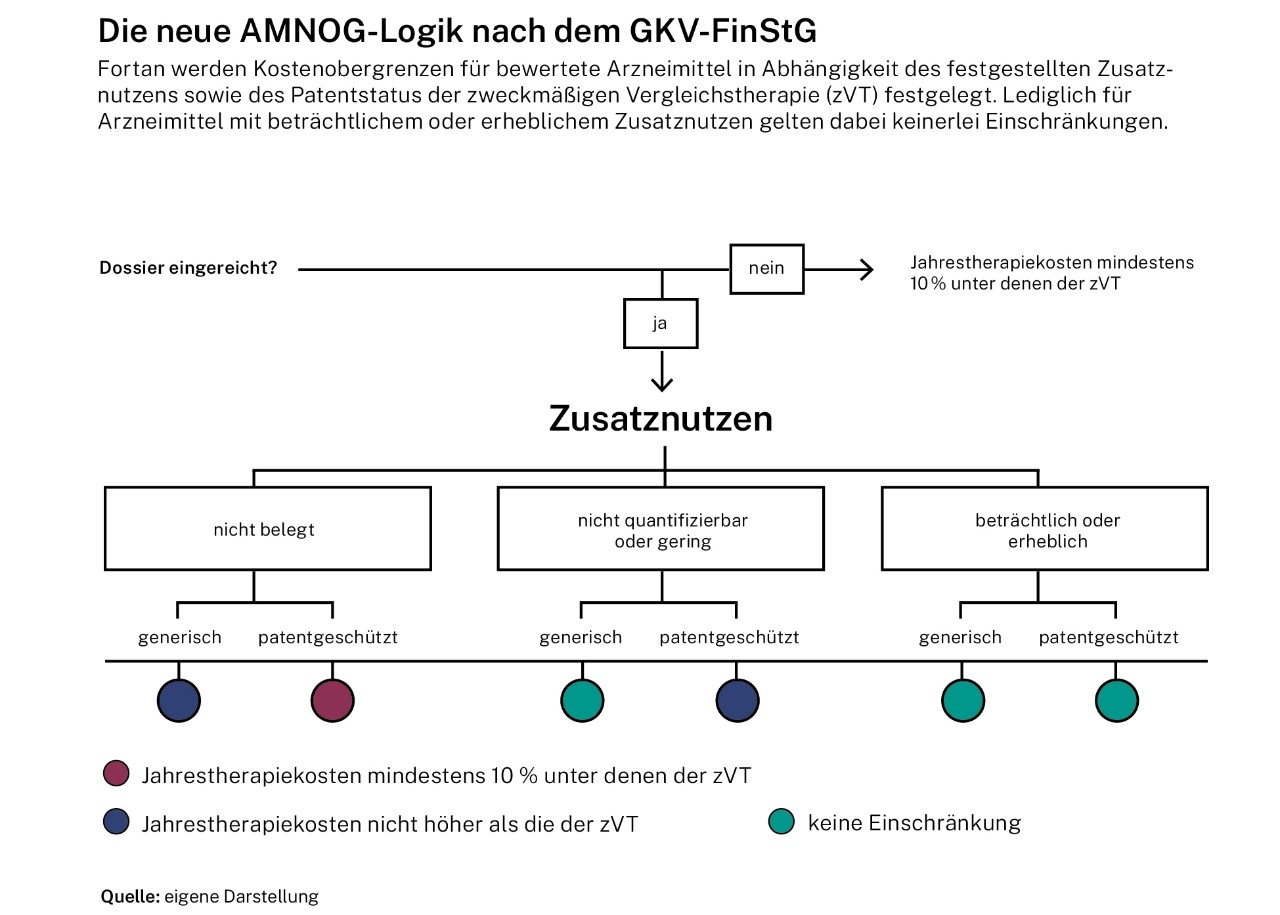
Eine weitestgehende Abkehr von der bisherigen AMNOG-Logik bedeuten die neuen Leitplanken für Erstattungsbeträge, welche angepasste Preisobergrenzen in Abhängigkeit der Vergleichstherapie und des Ergebnisses der Nutzenbewertung vorgeben. Der Grundsatz, dass ein Mehr an Nutzen auch zu einem höheren Preis berechtigt, gilt fortan nicht mehr bedingungslos. In erster Linie müssen die Leitplanken als Instrument gegen (hohe) Preissteigerungen bei Schrittinnovationen angesehen werden. Die Chance, die Ursachen der bestehenden Probleme etwa durch die Einbeziehung gesundheitsökonomischer Evaluationen in die Preisbildung zu beheben, wurde mit dem GKV-FinStG verpasst. Die Auswirkungen der neuen AMNOG-Logik sind derweil nur schwer abzuschätzen. Erste Modellberechnungen im AMNOG-Report zeigen jedoch, dass Leitplanken das Potenzial haben, zukünftig vier von fünf neuen Arzneimitteln zu betreffen und sehr wahrscheinlich auch höhere Einsparungen zu generieren, als dies bei der Gesetzgebung angenommen wurde. Angesichts dieser Unsicherheiten ist abzusehen, dass die Bewertung und Bepreisung von Arzneimitteln auch im Jahr 2023 für Diskussionsstoff sorgen wird.
Weitere Artikel aus ersatzkasse magazin. (2. Ausgabe 2023)
-
 Interview mit Manfred Lucha, Gesundheitsminister in Baden-Württemberg
Interview mit Manfred Lucha, Gesundheitsminister in Baden-Württemberg„Krankenhausplanung muss Sache der Länder bleiben“
-
 Interview mit Uwe Klemens, ehrenamtlicher Verbandsvorsitzender des vdek
Interview mit Uwe Klemens, ehrenamtlicher Verbandsvorsitzender des vdek„Die Sozialwahl ist eine Erfolgsgeschichte mit Zukunft“















 Gesunde Lebenswelten – Ein Angebot der Ersatzkassen
Gesunde Lebenswelten – Ein Angebot der Ersatzkassen Landesbasisfallwerte 2026
Landesbasisfallwerte 2026 ICF – Internationale Klassifikation der Funktionsfähigkeit, Behinderung und Gesundheit
ICF – Internationale Klassifikation der Funktionsfähigkeit, Behinderung und Gesundheit Beitragsbemessungsgrenzen und Beitragssätze 2026
Beitragsbemessungsgrenzen und Beitragssätze 2026 Heilmittelversorgung – Verträge und Vergütungen
Heilmittelversorgung – Verträge und Vergütungen


