Es ist viel in Bewegung gekommen bei der digitalen Gesundheitsversorgung. Mitte April 2020 hat das Bundesministerium für Gesundheit (BMG) den finalen Entwurf der Digitale-Gesundheitsanwendungen-Verordnung veröffentlicht. Damit wird das Digitale-Versorgung-Gesetz (DVG) im Hinblick auf die Prüfung und Zulassung von digitalen Gesundheitsanwendungen wie zum Beispiel Apps weiter konkretisiert. Ein vom Bundesinstitut für Arzneimittel und Medizinprodukte (BfArM) entwickelter Leitfaden schafft zusätzlich Transparenz.
Ein weiterer Schritt in Richtung digitaler Gesundheitsanwendungen (DiGA) ist geleistet, denn es besteht nun eine Rechtsgrundlage, die im Kern das Verfahren sowie die Anforderungen der Prüfung auf Erstattungsfähigkeit regelt. Seit dem In-Kraft-Treten des DVG am 19. Dezember 2019 besteht erstmals für mehr als 73 Millionen Versicherte in der gesetzlichen Krankenversicherung (GKV) ein Anspruch auf DiGA, die von Ärzten und Psychotherapeuten verordnet werden können und durch die Krankenkasse erstattet werden. Apps und Co. finden somit einen Weg in die Regelversorgung der GKV. Es ist davon auszugehen, dass die ersten DiGA ab August/September 2020 in die Versorgung gelangen. Dies wird entscheidend dazu beitragen, die Digitalisierung im Gesundheitswesen voranzubringen. Gerade die herausfordernden Zeiten der Corona-Pandemie haben gezeigt, wie wichtig digitale Lösungen in der Versorgung sind. Es muss jedoch sichergestellt werden, dass diese einen echten Mehrwert leisten. Ebenso bedarf es einer gründlichen Prüfung von Apps, beispielsweise im Hinblick auf den Datenschutz.
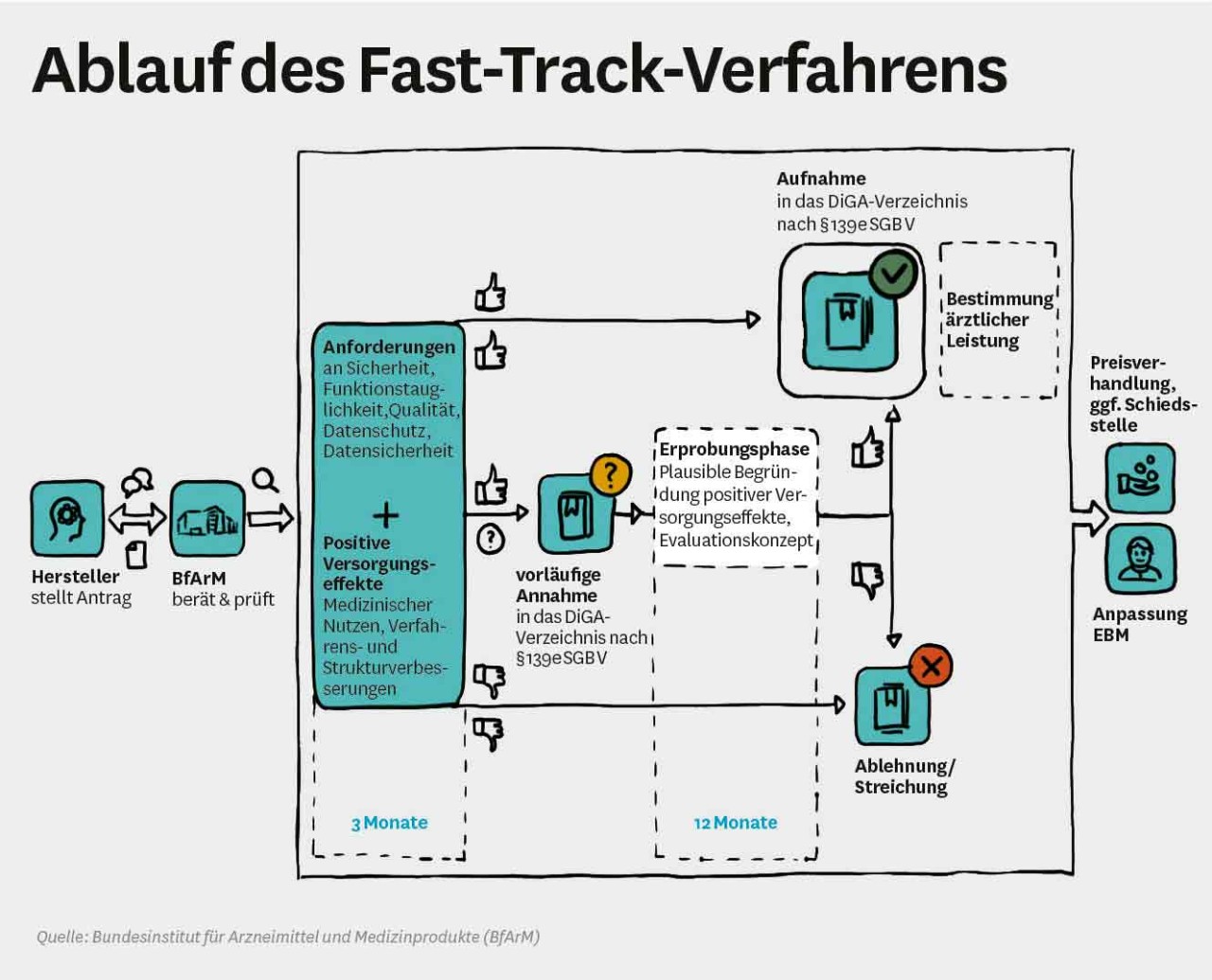
Schnelle Antragsprüfung durch Fast-Track-Verfahren
Bevor eine DiGA in die Versorgung gelangt und damit von den Krankenkassen erstattet werden kann, muss sie geprüft und zugelassen werden. Vorgesehen ist dafür das im DVG als zügig konzipierte Fast-Track-Verfahren. Anbieter von DiGA niedriger Risikoklassen müssen beim BfArM einen Antrag auf Aufnahme in ein Verzeichnis erstattungsfähiger Produkte stellen. Innerhalb von drei Monaten wird der Antrag geprüft und darüber entschieden, ob eine DiGA zugelassen wird. Welche Kriterien bei der Prüfung eine Rolle spielen und für die Zulassung ausschlaggebend sind, regelt die Rechtsverordnung. Zum einen müssen allgemeine Anforderungen, zum Beispiel im Hinblick auf Sicherheit und Funktionstauglichkeit, erfüllt werden. Zum anderen – und damit ausschlaggebend für die Zulassung als erstattungsfähiges Medizinprodukt – ist der Wirksamkeitsnachweis einer DiGA. Maßgeblich ist das Vorhandensein eines sogenannten positiven Versorgungseffektes für den Patienten.
Ein positiver Versorgungseffekt kann ein medizinischer Nutzen sein, beispielsweise die Verbesserung des Gesundheitszustandes. Aber es geht auch um patientenrelevante Struktur- und Verfahrensverbesserungen. Das bedeutet, dass eine DiGA beispielsweise die Koordination der Behandlungsabläufe verbessern oder den Zugang zur Versorgung erleichtern muss. Die Rechtsverordnung macht Vorgaben, wie die Kriterien, die zu einer Zulassung führen, nachzuweisen sind. Bei den allgemeinen Anforderungen an eine DiGA, beispielsweise im Hinblick auf Sicherheit, sieht die Verordnung Checklisten vor, die von den Herstellern auszufüllen sind. Um den Wirksamkeitsnachweis zu erbringen, sind dem BfArM Studien vorzulegen. Die Anforderungen an das Evidenzniveau sind jedoch in der Rechtsverordnung deutlich geringer als zum Beispiel in der Methoden- oder Arzneimittelbewertung durch den Gemeinsamen Bundesausschuss (G-BA). Der Nachweis kann bereits durch retrospektive Studien erfolgen. Deren Aussagekraft ist allerdings geringer als prospektive Studien, die man in der Rechtsverordnung hätte festschreiben können. Durch prospektive Studien wären die Hersteller verpflichtet worden, den Wirksamkeitsnachweis von DiGA mithilfe von Studien höherer Qualität zu erbringen. Das Fehlen der prospektiven Studien in der Verordnung ist zu kritisieren, da grundsätzlich verhindert werden muss, dass unwirksame DiGA in die Versorgung gelangen und damit erstattungsfähig sind.
Ergänzend zu der Rechtsverordnung hat das BfArM einen Leitfaden veröffentlicht. Dieser stellt eine zusammenfassende Darstellung der Regelungen der Rechtsverordnung dar. Es wird das Ziel verfolgt, eine verlässliche Handlungsgrundlage für die Antragstellung zu gewährleisten. Damit richtet sich der Leitfaden in erster Linie an Hersteller von DiGA. Auf 120 Seiten werden zentrale Aspekte erklärt, angefangen von der Einführung in das Fast-Track-Verfahren über die Anforderungen an eine DiGA bis hin zum Verfahren der Antragstellung. Versehen werden die Ausführungen dabei mit Hinweisen, Faustregeln und Beispielen aus der Praxis. Das ist positiv zu beurteilen, da somit Transparenz im Prüf- und Zulassungsverfahren des BfArM geschaffen wird. Der Leitfaden soll laufend aktualisiert werden.
Besonders wichtig ist außerdem die Frage der Vergütung einer DiGA. Hier hat der Gesetzgeber vorgegeben, dass der Preis im ersten Jahr vom Hersteller bestimmt werden kann. Erst nach Ablauf eines Jahres gelten zwischen dem GKV-Spitzenverband und dem Hersteller verhandelte Preise. Mit diesen Regelungen werden für die Anbieter erhebliche finanzielle Anreize geschaffen, ihre DiGA in den GKV-Leistungskatalog aufnehmen zu lassen; gleichzeitig besteht ein großes Risiko, dass sie im ersten Jahr dafür überhöhte Preise verlangen werden. Zur Verhinderung von Mondpreisen können die Hersteller der DiGA-Verbände und der GKV-Spitzenverband Höchstpreisregelungen vereinbaren. Sie sind dann Bestandteil einer Rahmenvereinbarung, die auch weitere Details der Preisverhandlungen regeln soll. An diesen Verhandlungen wird auch der Verband der Ersatzkassen e. V. (vdek) beteiligt sein.
Bereits im Gange sind Gespräche zwischen der GKV und der Kassenärztlichen Bundesvereinigung (KBV) zum zukünftigen Umgang mit ärztlichen Begleitleistungen. So können besondere Leistungen im Zusammenhang mit einer DiGA erforderlich sein, etwa spezifische Untersuchungen oder eine besondere Betreuung. Art und Umfang legt das BfArM fest, die Bewertung ist anschließend durch die Partner des Bundesmantelvertrages oder den Bewertungsausschuss zu regeln. Auch hierfür bedarf es bestimmter Rahmenbedingungen, die derzeit gemeinsam abgestimmt werden. Gleichzeitig befinden sich die Gespräche, wie konkret die Verordnung einer DiGA erfolgt und wie der Versicherte sie zukünftig erhalten kann, auf der Zielgerade. Es zeigt sich: An vielen Stellen wird derzeit daran gearbeitet, den Leistungsanspruch der Versicherten auf digitale Gesundheitsanwendungen zügig in die Tat umzusetzen. Nun kommt es auf die Hersteller an, dass die hochgesteckten Ziele an eine Verbesserung der Versorgung auch erreicht werden.
Weitere Artikel aus ersatzkasse magazin. 3. Ausgabe 2020
-
 Interview Prof. Dr. Steffen Augsberg (Deutscher Ethikrat)
Interview Prof. Dr. Steffen Augsberg (Deutscher Ethikrat)„Solidarität und Verantwortung sind keine unendlichen Ressourcen"










 Gesunde Lebenswelten – Ein Angebot der Ersatzkassen
Gesunde Lebenswelten – Ein Angebot der Ersatzkassen Landesbasisfallwerte 2026
Landesbasisfallwerte 2026 ICF – Internationale Klassifikation der Funktionsfähigkeit, Behinderung und Gesundheit
ICF – Internationale Klassifikation der Funktionsfähigkeit, Behinderung und Gesundheit Beitragsbemessungsgrenzen und Beitragssätze 2026
Beitragsbemessungsgrenzen und Beitragssätze 2026 Heilmittelversorgung – Verträge und Vergütungen
Heilmittelversorgung – Verträge und Vergütungen


